【英文名称】Sodium Hypochlorite
【分子式】NaOCl
【分子量】74.44
【CA登录号】7681-52-9
【缩写和别名】漂白剂
【物理性质】NaOCl-5H2O。mp 18°C,在水中的溶解度(0 °C)为293 g/L。该试剂多数情况下以水溶液形式使用。
【制备和商品】国内外化学试剂公司均有销售。将氯气通入到氢氧化钠溶液中即可得到次氯酸納的饱和溶液,含量为5.25 %。商业漂白剂的pH是11〜12.5,不需提纯可直接应用于有机反应。【注意事项】在储存过程中,高浓度的次氯酸钠溶
【注意事项】在储存过程中,高浓度的次氯酸钠溶液浓度会自动降低。固体次氯酸钠无论是在含有5个结晶水还是无水状态下均易发生爆炸。它也是一种强氧化剂,应避免与皮肤接触或吸入。
次氯酸钠(NaOCl)是有机合成中常用的氧化剂。它可以单独使用,但经常与其它助氧化剂或者催化剂一起使用,例如:2,2,6,6-四甲基哌啶-N-氧化物(TEMPO)和四丙基铵高钌酸盐(TPAP)。
NaOCl是一个受体系 pH 调控的试剂,商品漂白剂是一个很强的氧化剂。在β-环糊精的存在下,NaOCl 可以在水溶液中将伯醇和仲醇几乎定量地氧化成相应的醛和酮(式1)[1]。在乙酸溶液中,NaOCl 氧化能力得到调控以后可以在室温下将仲醇氧化成相应的酮。最重要的是:该反应可以在伯醇的存在下选择性地将仲醇氧化成相应的酮(式2和式3)[2~4]。

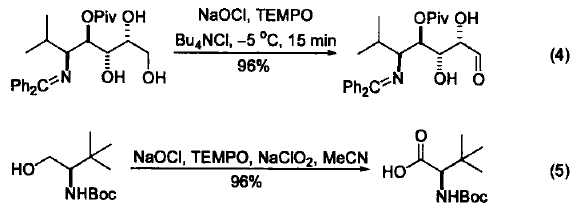
如果使用TEMPO作为共氧化剂与 NaOCl 一起使用,则可以在仲醇的存在下选择性地将伯醇氧化成相应的醛(式4)[5]。在 NaClO2 的存在下,该体系可以将伯醇氧化成相应的酸(式5)[7,8]。
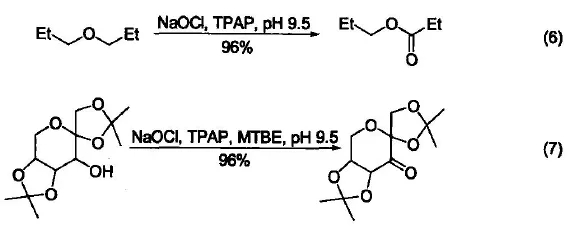
NaOCl与金属催化剂TPAP形成的组合试剂最值得关注,该体系显示出非常特别的氧化能力。例如:它可以将醚氧化成相应的酯(式6)[9]。又例如:在制备“史试剂”的过程中,许多氧化试剂不能将底物中的仲醇氧化成酮。但是,NaOCl/TPAP可以几乎定量地完成该转化过程(式7)[10]。
参考文献
1. Ji,H.; Shi, D.; Shao, M.; Li» Z.; Wang, L. Tetrahedron Lett. 2005,46,2517.
2. Stevens, R. V.; Chapman, K. T.; WeUer.H. N.7. Org. Chem. 1980,45,2030.
3. Stevens, R. V.; Chapman, K. T.; Stubbs, C. A.; Tam, W. W.; Albizati, K. F. Tetrahedron Lett. 1982,
23,4647.
4. Siedlecka, R.; Skarzewski, J.; Mlochowski, J. Tetrahedron Lett. 1990,31,2177.
5. Polt, R.; Sames, D.; Chnima, J. J. Org. Chem. 1999,64, 6147.
6. Leanna, M. R.; Sowin, T. J.; Morton, H. E. Tetrahedron Lett. 1992,33,5029.
7. Dettwiler, J. E.; Lubell, W. D. J. Org. Chem. 2003,68,177.
8. Cirimimia, R.; Pagliaro, M.; Blum, J.; Avnir,D. Chem. Commun. 2000,1441.
9. Gonsalvi, L.; Arends, I. W. C. E.; Moilanen, P.; Sheldon, R. A. Adv. Synth. Catal. 2003,345,1321.
10. Gonsalvi, L.; Arends, I. W. C. E.; Sheldon, R. A. Org. Lett. 2002,4, 1659.
关键词:氧化剂 次氯酸钠
分享至:
![]()
![]()




鄂公网安备 42011102004299号
© 2014-2025 前衍化学科技(武汉)有限公司 版权所有 鄂ICP备20009754号-1