实验目的
1、熟悉和掌握酯化反应的基本原理和制备方法,掌握可逆反应提高产率的措施; 2、掌握液体有机化合物的精制方法(分馏)。
实验内容
一、实验原理
在少量酸(H2SO4或HCl)催化下,羧酸和醇反应生成酯,这个反应叫做酯化反应(Esterification)。该反应通过加成-消去过程。质子活化的羰基被亲核的醇进攻发生加成,在酸作用下脱水成酯。该反应为可逆反应,为了完成反应一般采用大量过量的反应试剂(根据反应物的价格,过量酸或过量醇)。有时可以加入与水恒沸的物质不断从反应体系中带出水移动平衡(即减小产物的浓度)。在实验室中也可以采用分水器来完成。
酯化反应的可能历程为:
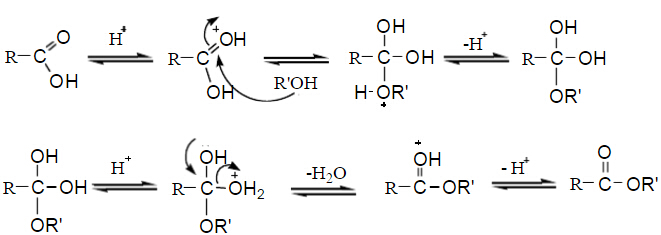
乙酸乙酯的合成方法很多,例如:可由乙酸或其衍生物与乙醇反应制取,也可由乙酸钠
与卤乙烷反应来合成等。其中最常用的方法是在酸催化下由乙酸和乙醇直接酯化法。常用浓硫酸、氯化氢、对甲苯磺酸或强酸性阳离子交换树脂等作催化剂。若用浓硫酸作催化剂,其用量是醇的3%即可。其反应为:

酯化反应为可逆反应,提高产率的措施为:一方面加入过量的乙醇,另一方面在反应过程中不断蒸出生成的产物和水,促进平衡向生成酯的方向移动。但是,酯和水或乙醇的共沸物沸点与乙醇接近,为了能蒸出生成的酯和水,又尽量使乙醇少蒸出来,本实验采用了较长的分馏柱进行分馏。
二、实验仪器及所需药品
仪器:恒压漏斗、三口圆底烧瓶、温度计、刺形分馏柱、蒸馏头、直形冷凝管、接引管
和锥形瓶。
药品:冰醋酸、95%乙醇、浓硫酸、饱和碳酸钠溶液、饱和食盐水、饱和氯化钙溶液、
无水碳酸钾。
三、主要试剂及产品的物理常数(文献值)
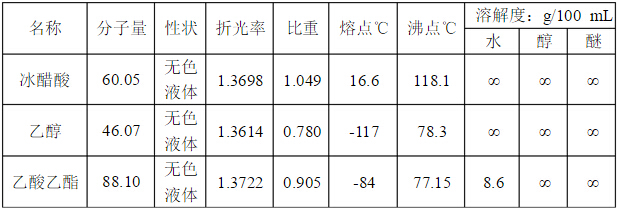
四、实验装置图
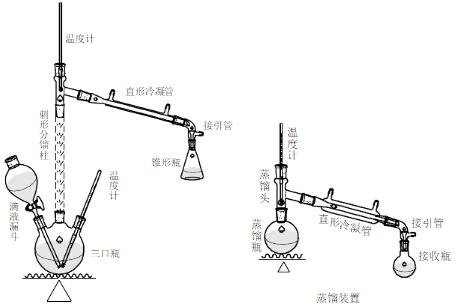
五、实验流程图
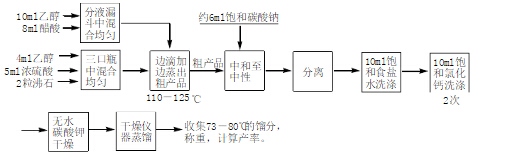
六、实验步骤
1、反应
在100 mL三口烧瓶中的一侧口装配一恒压滴液漏斗,滴液漏斗的下端通过一橡皮管连接一J形玻璃管,伸到三口烧瓶内离瓶底约3 mm处,另一侧口固定一个温度计,中口装配一分馏柱、蒸馏头、温度计及直型冷凝管。冷凝管的末对端连接接引管及锥形瓶,锥形瓶用冰水浴冷却。
在一小锥形瓶中放入3 mL乙醇,一边摇动,一边慢慢加入3 mL浓硫酸,并将此溶液倒入三口烧瓶中。配制15.5 mL乙醇和14.3 mL冰醋酸的混合溶液倒入滴液漏斗中。用油浴加热烧瓶,保持油浴温度在140℃左右,反应体系温度约为120℃左右。然后把滴液漏斗中的混合溶液慢慢滴加到三口烧瓶中。调节加料的速度,使和酯蒸出的速度大致相等。加料约90 min。这时保持反应物温度120~125℃。滴加完毕后,继续加热约10 min,直到不在有液体流出为止
2、纯化
反应完毕后,将饱和碳酸钠很缓慢地加入馏出液中,直到无二氧化碳气体逸出为止。饱和碳酸钠溶液要小量分批地加入,并要不断地摇动接收器(为什么?)。把混合液倒入分液漏斗钟,静置,放出下面的水层。用石蕊试纸检酯层。如果酯层仍显酸性,再用饱和然酸钠溶液洗涤,直到酯层不显酸性为止。用等体积的饱和食盐水洗涤(为什么?)。放出下层废液。从分液漏斗上口将乙酸乙酯倒入干燥的小锥形瓶内,加入无水碳酸钾干燥。放置约20min,在此期间要间歇震荡锥形瓶。
把干燥的粗乙酸乙酯滤入50mL烧瓶中。装配蒸馏装置,在水浴上加热蒸馏,收集74~80℃的馏分。
产量:14.5~16.5g
注意:
1、由于乙酸乙酯可以与水、醇形成二元、三元共沸物,因此在馏出液中还有水、乙醇;
2、在此用饱和NaCl溶液的目的是降低乙酸乙酯在水中的溶解度;
3、蒸馏:将干燥好的粗乙酸乙酯转移置50 mL的单口烧瓶中,水浴加热,常压蒸馏,收集
74~84℃馏分。称重并计算产率;
4、干燥剂无水碳酸钾也可用无水硫酸镁替代;
5、也可在石棉网上加热,控制反应温度在120~125℃,温度过高会增加副产物乙醚的含量;
6、控制浓硫酸滴加的速度太快,则会因局部放出大量的热量而引起爆沸;
7、洗涤时注意放气,有机层用饱和NaCl溶液洗涤后,尽量将水相分干净;
相关阅读
关键词:乙酸乙酯制备
分享至:
![]()
![]()




鄂公网安备 42011102004299号
© 2014-2025 前衍化学科技(武汉)有限公司 版权所有 鄂ICP备20009754号-1